গ্যাসগুলিকে তাদের আণবিক গঠন, আন্তঃঅণুর বল এবং ঘনত্বের উপর নির্ভর করে বাস্তব এবং আদর্শ হিসাবে শ্রেণীবদ্ধ করা যেতে পারে। এই নিবন্ধে, আমি আদর্শ গ্যাসের সূত্র এবং বাস্তব গ্যাসের ব্যত্যয় নিয়ে আলোচনা করব। আমি আন্তঃঅণুর বল এবং ঘনত্বের প্রভাবগুলিও পরীক্ষা করব। উপরন্তু, আমি সেই শর্তগুলি অনুসন্ধান করব যার অধীনে বাস্তব গ্যাস আদর্শ গ্যাসের মতো আচরণ করে। এই নিবন্ধটি আপনাকে গ্যাসের বিভিন্ন ধরণের মধ্যে পার্থক্য বুঝতে সাহায্য করবে এবং তাদের বৈশিষ্ট্য এবং আচরণ সম্পর্কে আরও জানতে সক্ষম করবে।
আদর্শ গ্যাসের সূত্র
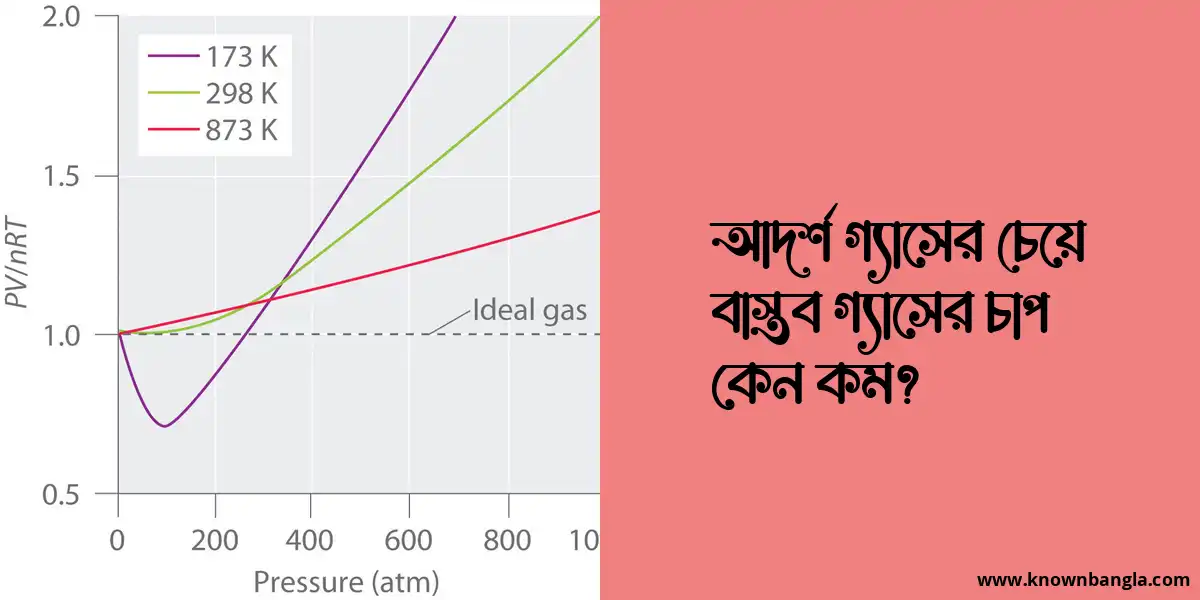
ে, আমরা অনুমান করি যে গ্যাসের অণুগুলি বিন্দু আকারের এবং এগুলির মধ্যে কোনো বল ক্রিয়া করে না। তবে, বাস্তব গ্যাসের অণুগুলির আয়তন থাকে এবং এগুলির মধ্যে আকর্ষণ ও বিকর্ষণ বল কাজ করে। এই বলগুলি বাস্তব গ্যাসের চাপকে আদর্শ গ্যাসের চাপের চেয়ে কম করে দেয়।
যখন বাস্তব গ্যাসকে সংকুচিত করা হয়, তখন অণুগুলি একে অপরের কাছাকাছি এসে যায় এবং আকর্ষণ বলের প্রভাব বৃদ্ধি পায়। এই আকর্ষণ বলগুলি গ্যাসের আয়তনকে হ্রাস করে এবং চাপ বাড়িয়ে তোলে। তবে, আদর্শ গ্যাসের মডেলে এই আকর্ষণ বলের প্রভাব উপেক্ষা করা হয়, যার কারণে আদর্শ গ্যাসের জন্য চাপের একটি কম মান পাওয়া যায়।
অন্যদিকে, যখন বাস্তব গ্যাসকে প্রসারিত করা হয়, তখন অণুগুলি একে অপরের থেকে দূরে সরে যায় এবং বিকর্ষণ বলের প্রভাব বৃদ্ধি পায়। এই বিকর্ষণ বলগুলি গ্যাসের আয়তনকে বাড়িয়ে দেয় এবং চাপ কমিয়ে দেয়। আদর্শ গ্যাসের মডেলে এই বিকর্ষণ বলের প্রভাবও উপেক্ষা করা হয়, যার কারণে আদর্শ গ্যাসের জন্য চাপের একটি বেশি মান পাওয়া যায়।
সুতরাং, বাস্তব গ্যাসের অণুগুলির আয়তন এবং এদের মধ্যকার বলের কারণে বাস্তব গ্যাসের চাপ আদর্শ গ্যাসের চেয়ে কম হয়।
বাস্তব গ্যাসের ব্যধান
আদর্শ গ্যাস সমীকরণটি বাস্তব গ্যাসের আচরণ বর্ণনা করতে ব্যবহৃত হয়। তবে উচ্চ চাপ এবং নিম্ন তাপমাত্রায়, বাস্তব গ্যাসের আচরণ আদর্শ গ্যাসের চেয়ে বিচ্ছিন্ন হতে পারে। এই বিচ্যুতিগুলি ঘটে কারণ আদর্শ গ্যাস সমীকরণ গ্যাস অণুগুলির মধ্যে আন্তঃআণবিক বল এবং গ্যাস অণুগুলির আয়তনকে উপেক্ষা করে।
বাস্তব গ্যাসের চাপ আদর্শ গ্যাসের চেয়ে কম হওয়ার প্রধান কারণ হচ্ছে আন্তঃআণবিক বল। উচ্চ চাপে, গ্যাস অণুগুলি একে অপরের খুব কাছে থাকে এবং আন্তঃআণবিক বলগুলি আর উপেক্ষা করা যায় না। এই বলগুলি গ্যাস অণুগুলিকে একে অপরের দিকে আকর্ষণ করে, যার ফলে গ্যাসের চাপ কমে যায়।
বাস্তব গ্যাসের চাপ আদর্শ গ্যাসের চেয়ে কম হওয়ার আরেকটি কারণ হচ্ছে অণুগুলির আয়তন। উচ্চ চাপে, গ্যাস অণুগুলির আয়তন আর অবহেলা করা যায় না। এই আয়তন গ্যাসের চাপের বিরুদ্ধে একটি প্রতিরোধের তৈরি করে, যা গ্যাসের চাপ কমিয়ে দেয়।
উচ্চ চাপ এবং নিম্ন তাপমাত্রায় বাস্তব গ্যাসের আচরণ কীভাবে পূর্বাভাস করা যায় তা বর্ণনা করার জন্য ভ্যান ডার ওয়ালস সমীকরণ সহ কয়েকটি সংশোধিত গ্যাস সমীকরণ রয়েছে। এই সমীকরণগুলি আন্তঃআণবিক বল এবং গ্যাস অণুগুলির আয়তনকে বিবেচনা করে এবং তাই উচ্চ চাপ এবং নিম্ন তাপমাত্রায় বাস্তব গ্যাসের আচরণের আরও সঠিক পূর্বাভাস দেয়।
আন্তঃঅণুর বলের প্রভাব
আদর্শ গ্যাস সমীকরণটি বাস্তব গ্যাসের আচরণ বর্ণনা করতে ব্যবহৃত হয়। তবে উচ্চ চাপ এবং নিম্ন তাপমাত্রায়, বাস্তব গ্যাসের আচরণ আদর্শ গ্যাসের চেয়ে বিচ্ছিন্ন হতে পারে। এই বিচ্যুতিগুলি ঘটে কারণ আদর্শ গ্যাস সমীকরণ গ্যাস অণুগুলির মধ্যে আন্তঃআণবিক বল এবং গ্যাস অণুগুলির আয়তনকে উপেক্ষা করে।
বাস্তব গ্যাসের চাপ আদর্শ গ্যাসের চেয়ে কম হওয়ার প্রধান কারণ হচ্ছে আন্তঃআণবিক বল। উচ্চ চাপে, গ্যাস অণুগুলি একে অপরের খুব কাছে থাকে এবং আন্তঃআণবিক বলগুলি আর উপেক্ষা করা যায় না। এই বলগুলি গ্যাস অণুগুলিকে একে অপরের দিকে আকর্ষণ করে, যার ফলে গ্যাসের চাপ কমে যায়।
বাস্তব গ্যাসের চাপ আদর্শ গ্যাসের চেয়ে কম হওয়ার আরেকটি কারণ হচ্ছে অণুগুলির আয়তন। উচ্চ চাপে, গ্যাস অণুগুলির আয়তন আর অবহেলা করা যায় না। এই আয়তন গ্যাসের চাপের বিরুদ্ধে একটি প্রতিরোধের তৈরি করে, যা গ্যাসের চাপ কমিয়ে দেয়।
উচ্চ চাপ এবং নিম্ন তাপমাত্রায় বাস্তব গ্যাসের আচরণ কীভাবে পূর্বাভাস করা যায় তা বর্ণনা করার জন্য ভ্যান ডার ওয়ালস সমীকরণ সহ কয়েকটি সংশোধিত গ্যাস সমীকরণ রয়েছে। এই সমীকরণগুলি আন্তঃআণবিক বল এবং গ্যাস অণুগুলির আয়তনকে বিবেচনা করে এবং তাই উচ্চ চাপ এবং নিম্ন তাপমাত্রায় বাস্তব গ্যাসের আচরণের আরও সঠিক পূর্বাভাস দেয়।
ঘনত্বের প্রভাব
আদর্শ গ্যাস সমীকরণটি বাস্তব গ্যাসের আচরণ বর্ণনা করতে ব্যবহৃত হয়। তবে উচ্চ চাপ এবং নিম্ন তাপমাত্রায়, বাস্তব গ্যাসের আচরণ আদর্শ গ্যাসের চেয়ে বিচ্ছিন্ন হতে পারে। এই বিচ্যুতিগুলি ঘটে কারণ আদর্শ গ্যাস সমীকরণ গ্যাস অণুগুলির মধ্যে আন্তঃআণবিক বল এবং গ্যাস অণুগুলির আয়তনকে উপেক্ষা করে।
বাস্তব গ্যাসের চাপ আদর্শ গ্যাসের চেয়ে কম হওয়ার প্রধান কারণ হচ্ছে আন্তঃআণবিক বল। উচ্চ চাপে, গ্যাস অণুগুলি একে অপরের খুব কাছে থাকে এবং আন্তঃআণবিক বলগুলি আর উপেক্ষা করা যায় না। এই বলগুলি গ্যাস অণুগুলিকে একে অপরের দিকে আকর্ষণ করে, যার ফলে গ্যাসের চাপ কমে যায়।
বাস্তব গ্যাসের চাপ আদর্শ গ্যাসের চেয়ে কম হওয়ার আরেকটি কারণ হচ্ছে অণুগুলির আয়তন। উচ্চ চাপে, গ্যাস অণুগুলির আয়তন আর অবহেলা করা যায় না। এই আয়তন গ্যাসের চাপের বিরুদ্ধে একটি প্রতিরোধের তৈরি করে, যা গ্যাসের চাপ কমিয়ে দেয়।
উচ্চ চাপ এবং নিম্ন তাপমাত্রায় বাস্তব গ্যাসের আচরণ কীভাবে পূর্বাভাস করা যায় তা বর্ণনা করার জন্য ভ্যান ডার ওয়ালস সমীকরণ সহ কয়েকটি সংশোধিত গ্যাস সমীকরণ রয়েছে। এই সমীকরণগুলি আন্তঃআণবিক বল এবং গ্যাস অণুগুলির আয়তনকে বিবেচনা করে এবং তাই উচ্চ চাপ এবং নিম্ন তাপমাত্রায় বাস্তব গ্যাসের আচরণের আরও সঠিক পূর্বাভাস দেয়।
যেসব শর্তে বাস্তব গ্যাস আদর্শ গ্যাসের মতো আচরণ করে
আদর্শ গ্যাস সমীকরণটি কেবল আদর্শ গ্যাসের ক্ষেত্রেই প্রযোজ্য। বাস্তব গ্যাসগুলি নিম্ন চাপ এবং উচ্চ তাপমাত্রায় আদর্শ গ্যাসের মতো আচরণ করে। যখন চাপ বাড়ে বা তাপমাত্রা কমে, তখন বাস্তব গ্যাসগুলি আদর্শ গ্যাসের মতো আচরণ করে না। বাস্তব গ্যাসের আচরণ আদর্শ গ্যাসের ক্ষেত্র থেকে বিচ্যুত হওয়ার কারণগুলি হল:
- আণবিক আকার: বাস্তব গ্যাসের অণুগুলির একটি নির্দিষ্ট আকার থাকে, যা আদর্শ গ্যাসের মডেলে উপেক্ষা করা হয়। এই আকারের কারণে অণুগুলির মধ্যে পারস্পরিক ক্রিয়া ঘটে, যা চাপ আদর্শ গ্যাসের চেয়ে কম করে।
- আন্তঃআণবিক বল: বাস্তব গ্যাসের অণুগুলির মধ্যে আন্তঃআণবিক বল থাকে, যেমন ভ্যান ডের ওয়ালস বল। এই বলগুলি অণুগুলিকে একে অপরের প্রতি আকর্ষণ করে, যা গ্যাসের চাপকেও কমায়।
- উচ্চ চাপ এবং নিম্ন তাপমাত্রা: উচ্চ চাপে এবং নিম্ন তাপমাত্রায়, বাস্তব গ্যাসের অণুগুলি এতটা কাছাকাছি এসে যায় যে তাদের স্বতন্ত্র আকার উপেক্ষা করা যায় না। এই ঘনস্থ অবস্থায়, অণুগুলির মধ্যে সংঘর্ষের ফ্রিকোয়েন্সি এবং তীব্রতা উভয়ই বৃদ্ধি পায়, যা চাপ বৃদ্ধি করে।






Leave a Reply